Miten silmäsairauksien potentiaalisia lääkehoitoja voidaan tutkia solumallin avulla?
Silmäsairaudet, kuten verkkokalvon irtauma, vaativat monipuolista hoitoa leikkauksista lääkitykseen. Tutkijat selvittivät solumallin avulla, onko kahdella lääkeaineella, simvastatiinilla ja amfenaakilla, kykyä vähentää silmän verkkokalvon tulehdusta, jos niitä annosteltaisiin suoraan soluille.
Johdanto
Silmäsairaudet ja näköön liittyvät haasteet ovat osa monen arkea. Yksi esimerkki on silmän verkkokalvon repeämä, joka johtaa tavallisimmin verkkokalvon irtaumaan. Verkkokalvon irtauma vaatii nopean leikkaushoidon, jota ilman irtauma voi johtaa sokeuteen. Irtaumassa verkkokalvo irtoaa silmän takaosassa paikaltaan aiheuttaen muun muassa hapen ja ravinteiden saannin puutteita. Leikkauksen jälkeisenä haittavaikutuksena voi syntyä sairaus nimeltä proliferatiivinen vitreoretinopatia (PVR), jossa verkkokalvolle muodostuu arpea. Arpeutuminen johtaa verkkokalvon rypistymiseen, uuteen irtaumaan ja uusintakirurgian tarpeeseen.
Silmän verkkokalvon pigmenttiepiteelisolut ja tulehdus ovat keskeisessä asemassa verkkokalvon irtaumassa ja proliferatiivisen vitreoretinopatian kehittymisessä.1 Siksi tutkimme kahden lääkeaineen, simvastatiinin ja amfenaakin, kykyä vähentää tulehdusta pigmenttiepiteelisoluissa. Pigmenttiepiteelisolut ovat verkkokalvolla näköreseptorien vieressä oleva yksisoluinen kerros, joka ylläpitää verkkokalvon tasapainoista toimintaa. Simvastatiini kuuluu statiineihin, jotka ovat kolesterolia alentavia lääkkeitä. Niiden on havaittu olevan potentiaalisia lääkeaineita, kun halutaan vähentää verkkokalvon irtauman uusintaleikkauksen tarvetta.2 Amfenaakki puolestaan on tulehduskipulääke, jota voidaan annostella esimerkiksi silmätippoina. Amfenaakin on todettu vähentävän esimerkiksi laserhoidon tarvetta kaihileikkauksen jälkeen.3 Tämän tutkimuksen tarkoitus oli selvittää pigmenttiepiteelisolumallin avulla, onko simvastatiinilla ja amfenaakilla vaikutuksia solujen tulehdusvasteisiin ja siten kykyä vähentää tulehdusta, jos niitä annosteltaisiin suoraan soluille.
Miten tutkimus tehtiin?
Teimme tutkimuksen ARPE-19 soluilla, jotka ovat alun perin 19-vuotiaana kuolleen miehen silmästä eristettyjä pigmenttiepiteelisoluja.4 ARPE-19 soluja käytetään yleisesti ihmisen silmän verkkokalvon sairauksien tutkimiseen, esimerkiksi selvitettäessä sairauksien syntymekanismeja ja potentiaalisia lääkehoitoja. Tutkimuksissa tarkastellaan lääkeaineiden soluvaikutuksia eli soluvasteita.
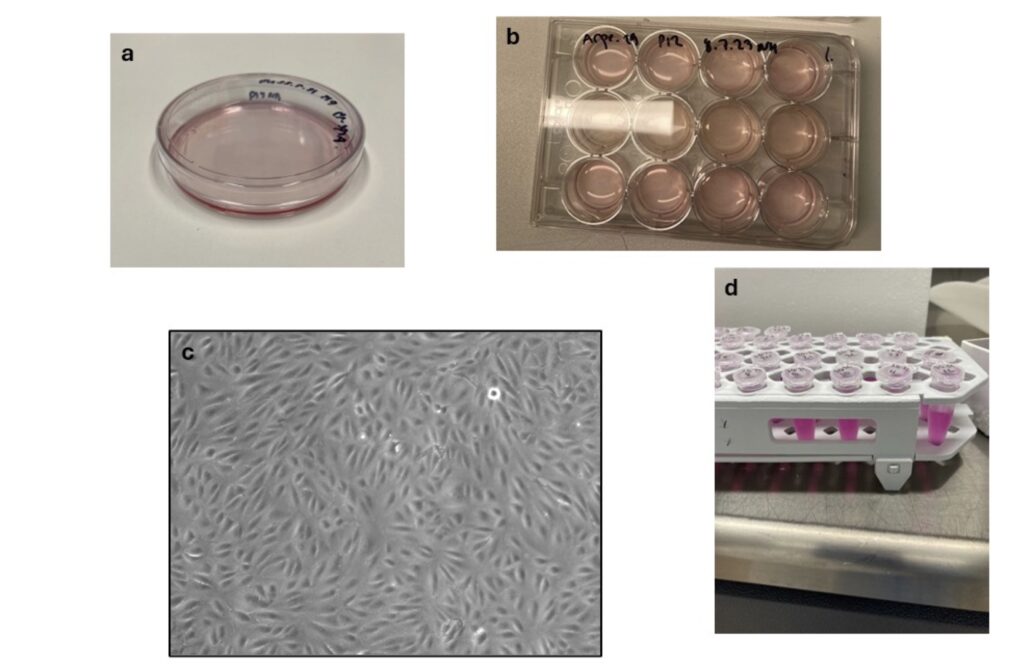
Ylläpidimme ARPE-19 soluja kasvustoilla (Kuva 1), joista jaoimme solut aina uusille ylläpitomaljoille kaksi kertaa viikossa. Kokeita varten jaoimme solut ylläpitomaljoilta varsinaisille koemaljoille (Kuva 1). Kasvatimme ARPE-19 soluja ihmisen elimistön olosuhteita muistuttavissa kasvatusolosuhteissa inkubaattorissa, jossa on 5 % hiilidioksidia, +37 ºC lämpötila ja kosteutta. Soluja kasvatetaan aluksi tyypillisesti 3 vuorokautta, jolloin ne saavuttavat niin sanotun konfluentin solukasvuston (Kuva 1), eli solut kasvavat koko maljan pohjalla. Tämän jälkeen soluja altistettiin ensin 24 tunnin ajan simvastatiinille ja amfenaakille, jonka jälkeen soluille tehtiin vielä 24 tunnin mittainen tulehdusta aiheuttava interleukiinikäsittely. Interleukiinit ovat solujen välisen tulehdusreaktion välittäjäaineita.
Näiden altistusten jälkeen kuvasimme solut mikroskoopilla ja keräsimme kasvatusliuoksen eli mediumin sekä solut erillisiin säilytysputkiin mittauksia varten (Kuva 1). Kasvatusliuos kerättiin pipetin avulla suoraan levyltä. Kerätyistä kasvatusliuosnäytteistä mittasimme solujen erittämiä tulehdusvälittäjäaineita kuten interleukiineja. Solut keräsimme lisäämällä niiden päälle fosfaattipuskuriliuosta, jonka jälkeen kaavimme ne liuoksesta säilytysputkiin ja pakastimme (-80 ºC) mittauksia varten. Solujen sisäisiä proteiinimittauksia varten solut tuli vielä hajottaa proteiinien vapauttamiseksi. Solujen hajotuksen teimme sitä varten optimoiduilla valmisteilla. Mittasimme solujen hajotuksesta saadun kokonaisproteiinimäärän ja käytimme loppuosan solujen proteiineista varsinaiseen mittaukseen. Osaa soluista käytimme myös solujen elinvoimaisuuden mittaamiseen tarkoituksena selvittää lääkeaineiden vaikutus solujen kuntoon, kuten mitokondrioiden toimintaan sekä solukalvon eheyteen. Siten jo tutkimuksen alussa varmistimme, etteivät tutkittavat lääkeaineet simvastatiini ja amfenaakki itsessään ole haitallisia solujen elävyydelle ja kunnolle.
Varsinaisissa mittauksissa käytimme erilaisia biokemiallisia menetelmiä. Hyödynsimme esimerkiksi erilaisia kolorimetrisia valmisteita, joissa reagenssien eli tiettyjen aineiden tai seoksien värimuutoksien perusteella mitattiin absorbanssitasoja. Absorbanssilla tarkoitetaan säteilyä, joka imeytyy aineeseen, kun sitä valaistaan tietyllä valon aallonpituudella. Suurin osa mittauksistamme perustui spektrofotometrin avulla tehtävään absorbanssin mittaukseen. Osa mittauksistamme perustui myös fluoresenssi-ilmiöön. Esimerkiksi kun mitataan solujen sisäisten happiradikaalien määrää, solut, jotka sisältävät suuremman määrän happiradikaaleja, tuottavat mittauksessa suuremman fluoresenssi-intensiteetin. Tyypillisin käyttämämme mittausmenetelmä oli entsyymivälitteinen immunosorbenttimääritys (engl. Enzyme-linked immunosorbent assay), jolla mitattiin muun muassa interleukiinien määrää kasvatusliuoksessa. Entsyymivälitteinen immunosorbenttimääritys on biokemiallinen menetelmä, jossa näytteestä määritetään vasta-aineen avulla tietty haluttu proteiini eli antigeeni. Kun vasta-aine ja antigeeni muodostavat sidoksen, sitä kutsutaan kompleksiksi. Vasta-aine-antigeenikompleksi tunnistetaan näytteestä reaktion osoittavien entsyymien avulla ja mittaamalla absorbanssitasoja spektrofotometrin avulla.
Mitä tutkimuksessa löydettiin?
Tutkimuksemme perusteella simvastatiini ja amfenaakki eivät olleet soluille haitallisia kokeellisesti aiheutetun tulehduksen aikana, koska solujen mitokondrioiden toimintakunto säilyi ja solukalvo ei hajonnut. Havaitsimme lieviä solukalvovaurioita lääkeaineiden yhteisvaikutuksessa. Solukuvien mukaan solut olivat kuitenkin hyväkuntoisen näköisiä. Etenkin simvastatiini osoitti monipuolisesti tulehdusta hillitsevää vaikutusta. Se vähensi solun tulehdusvälittäjäaineiden eritystä, kuten jo mainittuja interleukiineja. Simvastatiinin vaikutukset olivat havaittavissa myös silloin, kun soluja altistettiin samanaikaisesti amfenaakille. Amfenaakki ei yksinään osoittanut niin selkeää vaikutusta tulehdusvasteisiin, vaikka myös se hillitsi joitakin välittäjäaineita. Molemmille lääkeaineille oli ominaista lisätä solunsisäisten happiradikaalien määrää.
Tutkimustuloksista voidaan päätellä, että simvastatiini osoitti potentiaalia vähentää tulehdusvasteita ARPE-19 soluissa. Myös amfenaakki hillitsi tulehdusta, mutta hieman lievemmin. Yhdessä tai erikseen annosteltuna simvastatiini ja amfenaakki voivat hillitä pigmenttiepiteelisolujen tulehdusta ja siten mahdollisesti estää proliferatiivisen vitreoretinopatian muodostusta. Lääkeaineet tulisi kuitenkin saada kohdistettua verkkokalvon pigmenttiepiteelisoluihin, mikä tuo omat haasteensa. Näiden tutkimusten jälkeen emme voi vielä olla varmoja lääkkeiden todellisista vaikutuksista ja siksi tutkimuksia onkin syytä vielä jatkaa. Tutkimuksemme ovat solumalleilla tehtäviä, jolloin ei voida tehdä vielä suuria johtopäätöksiä mahdollisista vaikutuksista ihmisen silmässä.
Lopuksi
Tutkimuksemme mukaan simvastatiinilla ja amfenaakilla on tulehdusta vähentäviä vaikutuksia. Solunsisäisten happiradikaalien lisääntyminen on yleisesti mielletty haitalliseksi tapahtumaksi, mutta sen merkitystä kyseisten lääkeaineiden ja proliferatiivisen vitreoretinopatian tapauksessa on syytä tarkastella lisää. Todellisten vaikutusten selvittämiseksi lääkeaineita tulee tutkia myös muissa solumalleissa sekä tarkastella soluvasteita laajemminkin. Lisää tutkimuksia tarvitaan myös proliferatiivisen vitreoretinopatian syntymekanismeista, uusista potentiaalisista lääkeainevaihtoehdoista sekä erilaisten lääkeaineiden yhteisvaikutuksista. Solukokeet ovat tärkeitä tutkimusmenetelmiä sekä sairauden synnyn että mahdollisen lääkeaineen tutkimisessa. Ihmisen kokonaisuus on kuitenkin aina paljon monimutkaisempi, eivätkä solumallit yksinään kerro vielä koko totuutta.